دور الدبقية في الأمراض العصبية
منذ الاعتقاد بأن الخلايا الدبقية موجودة فقط لتقديم الدعم الهيكلي للخلايا العصبية ، وأكثر وأكثر يتم اكتشافها مع تردد أكبر أن هذه العناصر المجهرية تشارك بشكل كبير في الأداء الصحيح للجهاز العصبي. من بين الوظائف المعتادة التي تقوم بها الدبقية نجد الدفاع ضد الأضرار والغزاة ، وتغذية الخلايا العصبية أو تحسين الدافع الكهربائي ، مما يعني أنها أكثر بكثير من مجرد دعم بسيط في تطوير مثل هذه العصبونات و كما فكرت في الماضي.
من الدراسة المتنامية حول الدبقية ، نتطلع أيضًا إلى رؤية كيف أن هذه الخلايا (التي تمثل معظم مكونات الدماغ) تشارك في الأمراض العصبية والاضطرابات ، وهو شيء لم يتم القيام به حتى الآن إلا في التحقيق في أنواع مختلفة من الخلايا العصبية.
من المهم أن نفهم إلى أي مدى يتدخل العصبية في هذه العمليات ، لأن هذا قد يكون أحد الطرق لإيجاد العلاجات في المستقبل.
مراجعة سريعة: ما هو الدبقية؟
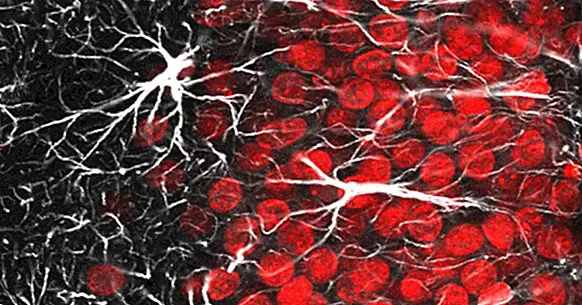
في الجهاز العصبي المركزي (CNS) نجد ثلاث فئات رئيسية من الخلايا الدبقية : oligodendrocytes ، المسؤولة عن وضع غمد المايلين على الخلايا العصبية. microglia ، التي تتمثل مهمتها في حماية الدماغ ؛ والخلايا النجمية ، والتي تقدم العديد من الوظائف لمساعدة الخلايا العصبية.
بخلاف SNC ، في الجهاز العصبي المحيطي (SNP) تم العثور على نوع رئيسي واحد فقط من الخلايا العصبية ، الخلايا الشائية wann ، والتي تنقسم إلى ثلاثة. أساسا ، فهي المسؤولة عن توليد طبقة المايلين في محاور العصبونات.
- لمعرفة المزيد حول هذا الموضوع ، يمكنك الرجوع إلى هذا المقال: "الخلايا الدبقية: أكثر بكثير من الغراء من الخلايا العصبية"
الأمراض والاضطرابات المرتبطة الدبقية
في الوقت الراهن، هناك أدلة متزايدة على أن العصبية تلعب دورا في الأمراض التي تؤثر على الجهاز العصبي المركزي ، سواء كانت جيدة أو سيئة. هنا أقدم قائمة صغيرة منهم ، تغطي أنواع مختلفة من الأمراض ، حيث أعلق على الآثار (التي هي معروفة في الوقت الحاضر) من الخلايا الدبقية فيها. من المحتمل أن يتم اكتشاف المزيد من التفاصيل في المستقبل.
1. الشلل الزمني والدائم
يعاني الشلل عندما يتم فقدان الاتصال بين الخلايا العصبية تليها الخلايا العصبية لأن "مسار الاتصال" الخاص بك قد تم كسره. من حيث المبدأ ، يمكن أن يطلق الدبقية المواد المعروفة باسم العصبونات العصبية التي تعزز نمو الخلايا العصبية. وكما هو الحال مع SNP ، فإن هذا يسمح للتنقل بالشفاء بمرور الوقت. لكن هذا ليس هو الحال في الجهاز العصبي المركزي ، الذي يعاني من شلل دائم.
لإثبات أن الدبقية متورطة في عدم الشفاء ، لأنها الشيء الوحيد الذي يميز هذا التغيير العصبي عندما يحدث في SNP أو في CNS ، ألبرت J. Aguayo ، الذي أجري في 1980s تجربة فيها الفئران مع الحبل الشوكي التالفة (أي ، مع الشلل) ، تلقوا زرع من الأنسجة العصبية الوركي نحو المنطقة المصابة. والنتيجة هي أنه في غضون شهرين ، عادت الفئران لتتحرك بكامل طبيعتها.
في التحقيقات اللاحقة ، تم العثور على أن هناك مجموعة من العوامل التي لا تسمح لاسترداد الكلي للارتباط. واحدة من هذه هي المايلين نفسها التي تنتجها الخلايا oligodendrocytes ، والتي عند تشكيل غمد ، يمنع نمو الخلايا العصبية . الهدف من هذه العملية غير معروف في الوقت الحالي. عامل آخر هو الأضرار الزائدة التي تولدها الخلايا الدبقية المكروية ، لأن المواد التي يتم إطلاقها للدفاع عن النظام تكون ضارة أيضًا للخلايا العصبية.
2. مرض كروتزفيلد جاكوب
ويتسبب هذا المرض العصبي من العدوى في البريون ، وهو بروتين غير طبيعي اكتسب الاستقلال الذاتي. اسم آخر يتلقاها هو اعتلال الدماغ الإسفنجى ، حيث أن دماغ هؤلاء المتأثرين ينتهي بكامل ثقوبه ، يعطي شعور الاسفنج. واحدة من المتغيرات لها تسبب في حالة تأهب صحية في التسعينيات ، والمعروفة باسم مرض جنون البقر.
إذا تم نقله ، فإنه يمتلك القدرة على عبور الحاجز الدموي الدماغي الانتقائي والإيواء في الدماغ. في الجهاز العصبي المركزي ، فإنه يصيب الخلايا العصبية وكذلك الخلايا النجمية والخلايا الدبقية المكروية ، وتكرار وقتل الخلايا وخلق المزيد والمزيد من بريون.
لم أنس النسيان ، ويبدو أن هذا النوع من الدبقية يقاوم العدوى بواسطة البريونات ، لكنه لا يتحمل الضرر التأكسدي التي تظهر كجزء من النضال الذي تقوم به الخلايا الدبقية الصغيرة في محاولة للدفاع عن الخلايا العصبية. في عام 2005 ، تم الإبلاغ عن أن البروتين في الحالة الطبيعية التي تولد البريون موجود في المايلين في الجهاز العصبي المركزي ، على الرغم من أن وظيفته غير معروفة.
3. التصلب الجانبي الضموري (ALS)
ALS هو مرض تنكسي يؤثر على الخلايا العصبية الحركية ، ويفقدون شيئا فشيئا وظائفهم ، مما تسبب في فقدان القدرة على الحركة حتى تصل إلى الشلل.
السبب هو طفرة في الجين الذي يشفر الإنزيم Superoxide Dismutase 1 (SOD1) ، الذي له وظيفة أساسية لبقاء الخلايا ، وهو القضاء على الجذور الحرة من الأكسجين. إن خطر الراديكاليين هو عدم توازن الشحنة في السيتوبلازم ، الأمر الذي يؤدي في نهاية المطاف إلى خلل خلوي وموت.
في تجربة مع الفئران مع متغير متحور من جين SOD1 ، كان ينظر إلى كيفية تطور مرض ALS. إذا تم منع الطفرة في الخلايا العصبية الحركية ، بقيت الفئران سليمة. ظهرت المفاجأة مع مجموعة التحكم ، حيث أظهرت الخلايا العصبية الحركية فقط الطفرة. تشير النظرية إلى أنه في هذه الفئران تموت العصبونات الحركية وتولد المرض. لكن هذا لم يحدث ، ولدهشة الجميع ، كانت الفئران سليمة على ما يبدو. الاستنتاج هو ذلك الخلايا بالقرب من الخلايا العصبية الحركية (الدبقية) لديها بعض الآليات المرتبطة بـ SOD1 يمنع التنكس العصبي.
على وجه الخصوص ، فإن المنقذين من الخلايا العصبية كانت الخلايا النجمية. إذا كانت العصبونات الحركية العصبية التي تنمو في اللوح مرتبطة مع الخلايا النجمية النقصية في SOD1 ، فإنها تموت. الاستنتاج المرسوم هو أن الخلايا النجمية الطافرة تطلق نوعًا من المادة السامة للعصبونات الحركية ، موضحًا لماذا تموت هذه الأنواع من العصبونات فقط في تطور المرض. بالطبع ، لا يزال العامل السام لغزا وموضوع التحقيق.
4. الألم المزمن
الألم المزمن هو اضطراب دائم تبقى خلايا الألم نشطة ، دون أي ضرر يسبب تحفيزهم . الألم المزمن يتطور عندما يكون هناك تغيير في دائرة الألم CNS بعد الإصابة أو المرض.
أشارت ليندا واتكنز ، وهي باحثة ألم في جامعة كولورادو ، إلى أن الخلايا الدبقية الصغيرة قد تكون متورطة في الألم المزمن من خلال قدرتها على إطلاق السيتوكينات ، وهي مادة تفرز استجابة التهابية وتنشط الألم.
للتحقق مما إذا كان على صواب ، أجري اختبارًا على الجرذان المصابة بألم مزمن ناجم عن تلف العمود الفقري. قاموا بإدارة مينوسايكلين ، الذي يستهدف الخلايا الدبقية المكروية ، ويمنع تنشيطها ، ونتيجة لذلك ، لا يطلق السيتوكينات. وكانت النتيجة فورية ، ولم تعد الجرذان تعاني من الألم .
وجدت مجموعة الدراسة نفسها الآلية التي يتعرف عليها الخلايا الدبقية الصغيرة عند تلف منطقة ما. الخلايا العصبية التالفة تطلق مادة تعرف باسم fractalkine ، أن الخلايا الدبقية الصغيرة تدرك وتدافع عن إفراز السيتوكينات . مشكلة الألم المزمن هي أنه لسبب ما ، لا تتوقف الخلايا الدبقية المكروية عن إطلاق السيتوكينات ، وتحفز باستمرار إنتاج الإحساس بالألم ، على الرغم من حقيقة أنه لا يوجد ضرر.
5. مرض الزهايمر
مرض الزهايمر هو مرض ذلك يدمر الخلايا العصبية وتواصلها ، مما يؤدي إلى فقدان الذاكرة . علامة على هذا المرض على تشريح الدماغ هو ظهور لويحات خرف في مناطق مختلفة من الدماغ. هذه اللويحات هي عبارة عن مجموعة من البروتينات تسمى بيتا اميلويد ، وهي سامة للخلايا العصبية.
من يولد هذا التراكم السام هو الخلايا النجمية. هذا النوع من الدبقية لديه القدرة على توليد الببتيد أميلويد بيتا ، لأنه يمكن أن يعالج سلفه ، بروتين اميلويد (APP). سبب هذا غير واضح بعد.
علامة أخرى هي أن حول لوحات تلاحظ كمية كبيرة من الخلايا الدبقية المكروية ، والتي في محاولة للدفاع عن الأنسجة ، يتم تجميعها لمكافحة تراكم الأميلويد بيتا وإطلاق المواد السامة (مثل السيتوكينات ، chemokines أو الأكسجين التفاعلي) ، والتي بدلا من أن تساعد ، تعزيز موت الخلايا العصبية ، كما أنها سامة بالنسبة لهم. بالإضافة إلى ذلك ، ليس لديهم أي تأثير على البلاك الخرفى.